
Produkt introduktion
| Calciumfluorid Grundlæggende information |
| Kemiske egenskaber krystalstruktur Anvender produktionsmetode |
| Produktnavn: | Calciumfluorid |
| Synonymer: | Calciumfluorid;Calciumfluorid, 99,9% spormetaller;Calciumfluorid, 99,95% spormetaller;Calciumfluorid, vandfrit, ampuleret under argon, 99,99% spormetaller;Calciumfluorid i kina)8 (ANTI-CNTEROT) produceret i kanin;CAF1-lignende protein;CALIFp |
| CAS: | 7789-75-5 |
| MF: | CaF2 |
| MW: | 78.07 |
| EINECS: | 232-188-7 |
| Produktkategorier: | Uorganiske stoffer;metalhalogenid |
| Mol fil: | 7789-75-5.mol |
 |
|
| Calciumfluorid Kemiske egenskaber |
| Smeltepunkt | 1402 grader |
| Kogepunkt | 2500 grader (belyst) |
| tæthed | 3,18 g/ml ved 25 grader (lit.) |
| brydningsindeks | 1.434 |
| Fp | 2500 grader |
| opbevarings temp. | -20 grad |
| opløselighed | Lidt opløselig i syre; uopløseligt i acetone. |
| form | stang |
| farve | hvid |
| Specifik vægtfylde | 3.18 |
| Vandopløselighed | 0,015 g. 100g H20 ved stuetemperatur.(UOPløselig) |
| Følsom | Hygroskopisk |
| Merck | 14,1667 |
| Opløselighed Produkt Konstant (Ksp) | pKsp: 8,28 |
| Eksponeringsgrænser | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2,5 mg/m3 |
| Dielektrisk konstant | 2,5 (omgivende) |
| Stabilitet: | Stabil. Calciumfluorid er inert over for organiske kemikalier og mange syrer, herunder HF. Det vil langsomt opløses i salpetersyre. |
| InChIKey | WUKWITHWXAAZEY-UHFFFAOYSA-L |
| CAS Database Reference | 7789-75-5(CAS Database Reference) |
| NIST Kemi Reference | Calciumfluorid(7789-75-5) |
| EPA stofregistreringssystem | Calciumdifluorid (7789-75-5) |
| Sikkerhedsoplysninger |
| Farekoder | Xi,Xn |
| Risikoerklæringer | 36/37/38 |
| Sikkerhedserklæringer | 26-37/39-36 |
| RIDADR | 3288 |
| WGK Tyskland | 1 |
| RTECS | EW1760000 |
| Farebemærkning | Irriterende |
| TSCA | Ja |
| HS kode | 28261900 |
| Data om farlige stoffer | 7789-75-5(data om farlige stoffer) |
| Toksicitet | LD50 ip i mus: 2638,27 mg/kg (Stratmann) |
| MSDS-oplysninger |
| Udbyder | Sprog |
|---|---|
| Calciumfluorid | engelsk |
| Sigma Aldrich | engelsk |
| ACROS | engelsk |
| ALFA | engelsk |
| Calciumfluorid brug og syntese |
| Kemiske egenskaber | Calciumfluorid er hovedingrediensen i flusspat eller fluorit, den kemiske formel er CaF2, det er farveløst kubisk krystal eller hvidt pulver. Den relative massefylde er 3,18, smeltepunktet er 1423 grader, kogepunktet er omkring 2500 grader. Opløseligheden i vand er minimal, 100 g vand kan kun opløse 0,0016 g ved 18 grader, det er uopløseligt i acetone, men opløseligt i saltsyre, flussyre, svovlsyre, salpetersyre og ammoniumsaltopløsning, og det kan ikke reagere med fortyndet syre, men kan reagere med varm koncentreret svovlsyre og danne flussyre, det kan danne et kompleks, når det opløses i aluminium og jernsalte (Fe3 +) opløsning. Naturligt calciumfluorid er mineralsk fluorit eller flusspat, viser ofte grå, gul, grøn, lilla og andre farver, nogle gange er det farveløst, gennemsigtigt, skinnende glas, skørt, og den relative tæthed er 3,01 ~ 3,25, det har et betydeligt fluorescensfænomen. Det kan bruges som kilde til fluor og materialet til at lave flussyresystem, fluorid; og det kan også bruges til fremstilling af glas, emalje, glasur. Fluorit bruges hovedsageligt som flusmiddel i metallurgi, den meget rene flusspat kan bruges til at lave speciallinser. Vand, når det indeholder (1~1,5) × 10-6 calciumfluorid, kan forhindre tandproblemer. Derudover kan det bruges til smeltning af jern og stål, kemikalier, glas, keramikfremstilling. Rent produkt kan bruges til katalysator for dehydrering, dehydrogenering. Ved virkningen af opløselige calciumsalte (calciumcarbonat eller calciumhydroxid) og natriumfluorid eller flussyre kan ammoniumfluorid, calciumfluorid opnås. |
| krystal struktur | Calciumfluorid er en ionisk krystal med fluoranionerne i et simpelt kubisk array og calciumkationer i halvdelen af strukturens kubiske steder. Calciumionerne kan også opfattes som værende på et "udvidet" fcc-gitter, hvor fluorionerne forårsager, at deres gitteradskillelse er 0.39 nm. Denne repræsentation er vist i det nederste diagram. Enhedscellen har 4 Ca2+ioner og 8 F1-ioner.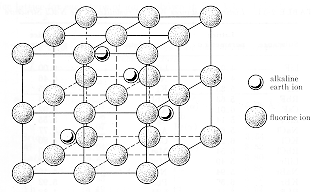 Materialet er gennemsigtigt i det synlige spektrale område, og viser elektronisk optisk adsorption i den ultraviolette og gitter optiske absorption i det infrarøde. |
| Bruger |
Industri
Anvendelse
Rolle/fordel
Kemisk fremstilling
Fremstilling af flussyre og fluorid
Råmateriale/kilde til fluor
Fremstilling af fluorfinkemikalier og syntetisk kryolit
Råmateriale/kilde til fluor
Arkitektonisk materiale
Fremstilling af glas
Fluxmiddel/fremme smeltning af råvarer
Fremstilling af cement
Mineraliseringsmiddel
Fremstilling af keramisk glasur
Fluxer og farvningshjælpemidler
Metallurgi
Jern- og stålsmeltning, ferrolegeringsproduktion osv.
Fluxmiddel/reducerer smeltepunktet for ildfaste stoffer
Medicin
Behandling, kontrol, forebyggelse og forbedring af allergiske reaktioner
Fremme ny knogledannelse
Termiske billeddannelsessystemer, spektroskopi, teleskoper og excimer-lasere
Fremstilling af optiske komponenter, såsom vinduer og linser
Råmateriale/bredt udvalg af transmissionslysfrekvenser; lavt brydningsindeks; høj termostabilitet
Andre
Produktion af svejsemidler
Vigtige komponenter i belægninger af svejsestave og svejsepulvere
Dehydrerings- og dehydrogeneringsreaktion
Katalysator/accelerer reaktionsprocessen
Fremstilling af bremsebelægning
Additiv/hjælper med at reducere slid forårsaget af høj varme og friktion
|
| Produktionsmetode | De fluoritaflejringer, der er blevet fundet i Kina, er primært brugt i minen ved hjælp af underjordiske minedriftsmetode, eller lavvandede åbne grubedrift, og underjordiske dybe minedrift, for malmlegemets mest vippeåre, udvidelsen er også stor. Minemetoden er baseret på et lavt hul. Krympningsmetoden er baseret. Mineprocessen ser "fosfatsten." Beneficieringsmetoder har generelt to typer, den ene er rå malm kan blive kvalificeret malmkoncentrat ved at håndtere udvalgte, den anden er håndvalgt mager malm og tailings. |
| Beskrivelse | Calciumfluorid er farveløst krystallinsk eller hvidt, pulveragtigt stof. Molekylvægt{{0}}.08;Specific gravity (H2O:1)=3.18 ved 20 grader ; Kogepunkt=2495 grad ; Fryse-/smeltepunkt=1423 grad . Fareidentifikation (baseret på NFPA-704 M-klassificeringssystem): Sundhed 2, Antændelighed 0, Reaktivitet 0. Praktisk talt uopløseligt vand. |
| Kemiske egenskaber | Calciumfluorid, CaF2, også kendt som fluorit og feldspat, er et farveløst fast stof sammensat af kubiske krystaller. Det har en lav vandopløselighed, men er let opløseligt i ammoniumsaltopløsninger. Calciumfluorid bruges til syntese af flussyre og i ætsningsglas. Calciumfluorid er ikke hygroskopisk og er relativt inert. Den har en tilstrækkelig høj modstandsdygtighed over for termiske og mekaniske stød, og den kan let fremstilles i en række forskellige detektorgeometrier. Calciumfluorid har et meget lavt damptryk, hvilket gør det muligt at bruge det i en bred vifte af vakuumapplikationer. Det er uopløseligt i vand og de fleste organiske opløsningsmidler, hvilket gør det muligt at placere radioaktive prøver i opløsning i direkte kontakt med krystallen. Calciumfluorid er et gennemsigtigt materiale, der bruges til at detektere -stråler op til flere hundrede keV og til at detektere ladede partikler. På grund af dets lave atomnummer er materialets fotofraktion relativt lille, hvilket begrænser dets anvendelse i strålespektrometri ved højere energier. Men det lave atomnummer gør calciumfluorid til et ideelt materiale til påvisning af -partikler på grund af den lille mængde tilbagespredning. |
| Fysiske egenskaber | Hvid kubisk krystal eller pulver; brydningsindeks 1,434; massefylde 3,18 g/cm3; hårdhed 4 Mohs; smelter ved 1.418 grader; fordamper ved 2.533 grader; uopløselig i vand (16 mg/L ved 20 grader); Ksp 3,9x10-11; let opløselig i fortyndet mineralsyre; opløselig i koncentrerede syrer (med reaktion). |
| Bruger | Naturligt forekommende CaF2 er den vigtigste kilde til hydrogenfluorid, et råstofkemikalie, der bruges til at fremstille en lang række materialer. Fluor frigives fra mineralet ved indvirkning af koncentreret svovlsyre: CaF2 (fast)+H2SO4 (flydende)→CaSO4 (fast)+2HF (gas) CaF2 bruges som en optisk komponent på grund af dets kemiske stabilitet under ugunstige forhold. Calciumfluorid bruges almindeligvis som vinduesmateriale til både infrarøde og ultraviolette bølgelængder, da det er gennemsigtigt i disse områder (ca. 0.15 til 9 mm) og udviser et ekstremt lavt brydningsindeks. Calciumfluorid er en vanduopløselig calciumkilde til brug i iltfølsomme applikationer, såsom metalproduktion. I ekstremt lave koncentrationer (ppm) anvendes fluorforbindelser i sundhedsapplikationer. Fluorforbindelser har også betydelige anvendelser i syntetisk organisk kemi. De er også almindeligt anvendt til legering af metal og til optisk aflejring. Det bruges også som flusmiddel til smeltning og væskebehandling af jern, stål og deres kompositter. Dets virkning er baseret på dets smeltepunkt, der ligner jern, på dets evne til at opløse oxider og på dets evne til at fugte oxider og metaller. |
| Bruger | Fluorspat er den primære kilde til fluor og dets forbindelser. I jernmetallurgi bruges det som et flusmiddel for at øge slaggens fluiditet. Stålindustrien er den største forbruger; den kemiske industri, andet og glas og keramik, tredje. Syntetisk flusspat bruges i den optiske industri (transmitterer uv-stråler), og ren calciumfluorid bruges som katalysator ved dehydrering og dehydrogenering. Bruges til at fluoridere drikkevand. |
| Bruger | Calciumfluorid er den kommercielt vigtige kilde til fluorforbindelser såvel som hydrogenfluorid. Det er gennemsigtigt fra ultraviolet til infrarødt område. Det bruges i spektroskopi, termiske billeddannelsessystemer og excimer-lasere; det bruges også til fremstilling af optiske komponenter, herunder vinduer, prismer og linser. Derudover bruges det også i aluminiummetallurgi, bremsebelægningsfremstillingsindustrier og i tandemalje. |
| Definition | En ren naturligt forekommende form for calciumfluorid. |
| Produktionsmetoder | Det kommercielle produkt er fremstillet af naturligt forekommende mineralsk flusspat, som renses og pulveriseres. Det kan også udfældes ved at blande en opløsning af natriumfluorid med et opløseligt calciumsalt: Ca(NEJ3)2+ 2NaF → CaF2+ NaNO3 Alternativt kan det opnås ved at behandle calciumcarbonat med flussyre:CaCO3+ 2HF → CaF2+ CO2 + H2O. |
| Definition | En mineralsk form for calciumfluorid (CaF2), brugt til fremstilling af nogle cementer og glastyper. |
| Generel beskrivelse | Lugtfrit gråt pulver eller granulat. Synker i vand. |
| Reaktivitetsprofil | Calciumfluorid har svage oxiderende eller reducerende egenskaber. Redoxreaktioner kan dog stadig forekomme. Størstedelen af forbindelserne i denne klasse er svagt opløselige eller uopløselige i vand. Hvis de er opløselige i vand, er opløsningerne sædvanligvis hverken stærkt sure eller stærkt basiske. Disse forbindelser er ikke vand-reaktive. |
| Fare | Et irritationsmoment. |
| Sundhedsfare | Lille akut toksicitet |
| Antændelighed og eksplosionsevne | Ikke brandfarlig |
| Industrielle anvendelser | Også kaldet fluorit, flusspat er et krystallinsk eller massivt granulært mineral af sammensætningen CaF2, brugt som flusmiddel ved fremstilling af stål, til fremstilling af flussyre, i opaliserende glas, i keramiske emaljer, til slyngning af kunstig kryolit, som bindemiddel til glasagtige slibeskiver og til fremstilling af hvid cement. Det er et bedre flusmiddel for stål end kalksten, hvilket gør en flydende slagge og frigør jernet for svovl og fosfor. Syrespat er en kvalitet, der bruges til fremstilling af flussyre. Det bruges også til fremstilling af kølemidler, plastik og kemikalier og til aluminiumreduktion. Optisk flusspat er den højeste kvalitet, men er ikke almindelig. Fluorkrystaller til optiske linser dyrkes kunstigt af syre-grade flusspat. Ren calciumfluorid, Ca2F6, er et farveløst krystallinsk pulver, der bruges til ætsning af glas, i emaljer og til at reducere friktionen i maskinlejer. Det bruges også til keramiske dele, der er modstandsdygtige over for flussyre og de fleste andre syrer. Calciumfluorit har silicium i molekylet og er et krystallinsk pulver, der bruges til emaljer. De klare rombefluoridkrystaller, der bruges til at omdanne elektrisk energi til lys, er blyfluorid, PbF2. |
| Sikkerhedsprofil | Moderat giftig ved intraperitoneal vej. Mildt giftig ved indtagelse. Et eksperimentelt teratogent. Andre eksperimentelle reproduktive effekter. Mutationsdata rapporteret. Se også FLUORIDER OG CALCIUMFORBINDELSER. Når den opvarmes til nedbrydning, udsender den giftige dampe af F-. |
| Potentiel eksponering | Calciumfluorid bruges til fremstilling af flussyre; som et flusmiddel i stålfremstilling; i smeltning; elektrisk lysbuesvejsning, fremstilling af glas og keramik; og at fluoridere drikkevand. |
| Førstehjælp | Hvis dette kemikalie kommer ind i øjnene, skal du fjerne eventuelle kontaktlinser med det samme og skylle straks i mindst 15 minutter, og lejlighedsvis løfte øvre og nedre øjenlåg. Søg straks lægehjælp. Hvis dette kemikalie kommer i kontakt med huden, skal du fjerne forurenet tøj og straks vaske det med vand og sæbe. Søg straks lægehjælp. Hvis dette kemikalie er blevet inhaleret, skal du fjerne det fra eksponeringen, begynde at redde vejrtrækningen (ved at bruge universelle forholdsregler, inklusive genoplivningsmaske), hvis vejrtrækningen er stoppet og HLR, hvis hjerteaktiviteten er stoppet. Overfør omgående til en medicinsk facilitet. Søg lægehjælp, når dette kemikalie er blevet slugt. En læge eller autoriseret paramediciner kan overveje at indgive aluminiumhydroxidgel, hvis han er ved bevidsthed. |
| opbevaring | Farvekode-grøn: Generel opbevaring kan bruges. Opbevares i tæt lukkede beholdere på et køligt, godt ventileret område væk fra syrer og kemisk aktive metaller (såsom kalium, natrium, magnesium og zink), fordi der vil blive produceret ætsende hydrogenfluorid. |
| Forsendelse | Calciumfluorid er ikke specifikt dækket af DOT i dets Performance-Oriented Packaging Standards. |
| Uforeneligheder | Støv kan danne eksplosiv blanding med luft. Reagerer med vand, fugtig luft og damp og frigiver brændbar brintgas; og kan selvantænde i luften. Et stærkt reduktionsmiddel; inkompatibel med oxidationsmidler (chlorater, nitrater, peroxider, permanganater, perklorater, klor, brom, fluor osv.); kontakt kan forårsage brand eller eksplosioner. Holdes væk fra alkaliske materialer, stærke baser, stærke syrer, oxosyrer, epoxider. Inkompatibel med metalhalogenater, sølvfluorid og tetrahydrofuran |
| Calciumfluorid præparationsprodukter og råvarer |
| Råvarer | Hydrogen fluoride-->Calcium hydroxide-->CARBON MONOXIDE-->Quartz-->Calcium acetate-->calciummagnesiumphosphat (CMP) |
| Forberedelsesprodukter | Hydrogen fluoride-->Boron trifluoride diethyl etherate-->Potassium Phosphate Monobasic-->Hexafluorosilicic acid-->Calcium cyanamide-->Sodium fluoride-->Trisodium hexafluoroaluminate-->Aluminum fluoride-->bastnasite-->Carbon tetrafluoride-->cryolite-->ZINC SILICOFLUORIDE-->MAGNESIUM HEXAFLUORACTYLACETONAT DIHYDRAT |
Populære tags: calciumfluorid, Kina calciumfluorid fabrikanter, leverandører, fabrik
Et par af: Zinkfluorid
Næste: Strontiumfluorid
Du kan også lide
Send forespørgsel


