
Produkt introduktion
| Aluminiumfluorid Grundlæggende information |
| Beskrivelse Syntese Anvendelse Toksikologiske undersøgelser Sikkerhedsreferencer |
| Produktnavn: | Aluminium fluorid |
| Synonymer: | fluoridhlinitet;ALUMINIUM TRIFLUORID;ALUMINIUM FLUORIDE;Aluminiumtrifluorid;ALUMINIUM FLUORIDE;ALUMINIUM(III) FLUORID;Aluminiumfluorid,99.9+%,ren;ALUMINIUM FLUORIDE H |
| CAS: | 7784-18-1 |
| MF: | AlF3 |
| MW: | 83.98 |
| EINECS: | 232-051-1 |
| Produktkategorier: | metalhalogenid; uorganiske stoffer; uorganiske fluorider; aluminiumsalte; aluminiummetal og keramisk videnskab; krystalkvalitet uorganiske stoffer; metal og keramik videnskab; salte |
| Mol fil: | 7784-18-1.mol |
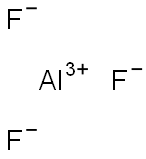 |
|
| Aluminiumfluorid kemiske egenskaber |
| Smeltepunkt | 1290 grader (belyst) |
| Kogepunkt | 1291 grader |
| tæthed | 3,1 g/ml ved 25 grader (lit.) |
| Fp | 1250 grader |
| opløselighed | Svagt opløseligt i syrer og baser. Uopløseligt i acetone. |
| form | pulver |
| farve | Hvid til lysegrå |
| Specifik vægtfylde | 2.882 |
| Vandopløselighed | LIDT OPLØSELIG |
| Følsom | Hygroskopisk |
| Sublimering | 1250 ºC |
| Merck | 14,339 |
| Eksponeringsgrænser | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2 mg/m3; TWA 2,5 mg/m3 |
| Dielektrisk konstant | 2.2 (omgivende) |
| CAS DataBase Reference | 7784-18-1(CAS DataBase Reference) |
| NIST Kemi Reference | Aluminiumtrifluorid(7784-18-1) |
| EPA stofregistreringssystem | Aluminiumtrifluorid (7784-18-1) |
| Sikkerhedsoplysninger |
| Farekoder | Xn,T,Xi |
| Risikoerklæringer | 22-36/37/38 |
| Sikkerhedserklæringer | 26-37/39 |
| RIDADR | 3260 |
| WGK Tyskland | 1 |
| RTECS | BD0725000 |
| Farebemærkning | Meget giftig/irriterende |
| TSCA | Ja |
| Fareklasse | 8 |
| Pakkegruppe | III |
| HS kode | 28261210 |
| Data om farlige stoffer | 7784-18-1(data om farlige stoffer) |
| MSDS-oplysninger |
| Udbyder | Sprog |
|---|---|
| Aluminium fluorid | engelsk |
| Sigma Aldrich | engelsk |
| ACROS | engelsk |
| ALFA | engelsk |
| Brug og syntese af aluminiumfluorid |
| Beskrivelse | Aluminiumfluorid er i form af hvidt krystallinsk fast stof eller et hvidt pulver. Det forekommer naturligt som mineraler rosenbergit og oskarssonit.1 Det kan også fremstilles syntetisk. |
| Syntese | Aluminiumfluorid fremstilles ved metoder i følgende: 1) Flukiselsyre med aluminiumhydroxid2 H2SiF6 + 2 Al(OH)3 → 2 AlF3 + SiO2 + 4 H2O (I) Reaktionen er eksoterm og forløber i flere trin. Det kan beskrives ved følgende tre reaktioner: 3H2SiF6 + 2 Al(OH)3 → Al2(SiF6)3 + 6 H2O (II) Al2(SiF6)3 + 6 H2O → 2 AlF3 + 3 SiO2 + 12 HF (III) 12 HF + 4 Al(OH)3 → 4 AlF3 + 12 H2O Reaktionen udføres mellem 70°C og 100°C. Koncentrationen af fluorkiselsyre kan være så høj som 35 vægt% i en vandopløsning. Da den fremstillede aluminiumfluoridopløsning er metastabil, og trihydratet begynder at krystallisere hurtigt ud ved temperatur omkring 90°C, skal udfældet fast silica fjernes så hurtigt som muligt. 2) Al2O3 med vandig flussyre3 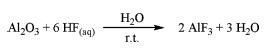 Flussyre tilsættes dråbevis under kraftig omrøring ved stuetemperatur til Al2O3-suspensionen. Efterfølgende er det faste oxid fuldstændigt opløst. Den resulterende klare opløsning omrøres i dagevis ved stuetemperatur. I løbet af denne periode separeres de hvide faste bundfald fra opløsningsmidlet, vaskes med vand og tørres efterfølgende. Efter behandling i en muffelovn ved den ønskede kalcineringstemperatur opnås aluminiumfluorid. 3) Aluminiumalkoxid med ikke-vandig HF-opløsning4 Aluminiumalkoxid, Al(OR)3 (R=Me, Et, iPr eller tBu), reagerer med ikke-vandig HF-opløsning i et organisk opløsningsmiddel. Reaktionen udføres i en sol-gel-tilstand. Efter ældning dannes et fast stof, som sætter sig. Det faste stof fraskilles ved centrifugering og tørres under vakuum. Gasfasefluorering af den tørrede gel påføres derefter for at opnå aluminiumfluorid. |
| Anvendelse | Aluminiumfluorid er et af de vigtigste tilsætningsstoffer i den industrielle produktion af aluminium. Brugen af aluminiumfluorid kan sænke kryolittens smeltepunkt og forbedre elektrolyttens fysiske og kemiske egenskaber. I aluminiumproduktionen opløses aluminiumoxid i en opløsning af kryolit. Ved at lede en elektrisk strøm gennem opløsningen produceres aluminium. Ikke desto mindre smelter kryolitopløsning ved omkring 1000 grader. Når aluminiumfluorid tilsættes, kan elektrolyse ske i kryolitopløsningen ved en temperatur 40-60 grad lavere, hvilket reducerer den nødvendige mængde energi til at producere aluminium.5 Aluminiumfluorid bruges som et barrierelag for at forsinke oxidation af aluminiumsspejle. 6 Det bruges som flusmiddel i keramiske glasurer og emaljer, til fremstilling af aluminiumsilikat og som katalysator. Aluminiumfluoridkomplekser med proteiner kan bruges til at studere de mekanistiske aspekter af fosforyloverførselsreaktioner i biologi, som er af fundamental betydning, da fosforsyreanhydrider som ATP og GTP styrer de fleste af de reaktioner, der er involveret i metabolisme, vækst og differentiering.8 Aluminiumfluorid bruges sammen med zirconiumfluorid til fremstilling af fluoroaluminatglas. I landbruget kan aluminiumfluorid bruges til at hæmme gæringen. Fysisk dampaflejret aluminiumfluorid kan bruges som en optisk tynd film med lavt indeks i situationer, hvor der kræves langt UV-gennemsigtighed.1 |
| Toksikologiske undersøgelser | Oral dyredødelig dosis (LD50) af aluminiumfluorid er 0,1 g/kg. Aluminiumfluorid er mindre giftigt end de fleste fluorider på grund af dets ringe vandopløselighed. Udsættelse for høje koncentrationer af aluminiumfluorid forårsager hypocalcæmi. Indånding og indtagelse af aluminiumfluorid resulterer i typiske symptomer på fluorforgiftning. Symptomer på alvorlig forgiftning omfatter åndenød, overbelastning af lungerne, muskelspasmer og kramper.8 Akutte (kortvarige) toksiske virkninger kan omfatte død af dyr, fugle eller fisk og død eller lav vækstrate hos planter. Akutte virkninger observeres i 2 til 4 dage efter eksponering af dyr eller planter for aluminiumfluorid. Kroniske (langsigtede) toksiske effekter kan omfatte forkortet levetid, reproduktionsproblemer, lavere fertilitet og ændringer i udseende eller adfærd hos udsatte dyr. |
| Sikkerhed | Aluminiumfluorid er et ikke-brændbart fast stof. Men det er uforeneligt med mange andre råvarer, herunder kemisk aktive metaller (f.eks. kalium og natrium), syre og sure dampe. Kontakt kan forårsage brand eller eksplosion. Ved opvarmning kan der udsendes giftige dampe af fluor, herunder ekstremt giftig hydrogenfluorid. |
| Referencer |
https://en.wikipedia.org/wiki/Aluminium_fluorid John Karlström, reaktormodel til fremstilling af aluminiumfluorid W. Kleist, C. Häßner, O. Storcheva, K. Köhler, En simpel vandig fasesyntese af aluminiumfluorid med stort overfladeareal og dets bulk og overfladestruktur, Inorganica Chimica Acta, 2006, vol. 359, s. 4851-4854 SK Ruediger, U. Groß, M. Feist, H A. Proscott, SC Shekar, SI Troyanov, E. Kemnitz, Ikke-vandig syntese af mekanistisk undersøgelse af aluminiumfluoridea med højt overfladeareal, Journal of Materials Chemistry, 2005, vol. 15, s. 588-597 https://info.noahtech.com R. Elaish, M. Curioni, K. Gowers, A. Kasuga, H. Habazaki, T. Hashimoto, P. Skeldon, Elelctrochimica Acta, 2017, vol. 245, s. 854-862 Alfred Wittinghofer, Signalmekanik: Aluminiumfluorid for årets molekyle, 1997, vol. 7, s. R682-R685 Jeffrey Wayne Vincoli, Risk Management for Hazardous Chemicals, Bund 1, 1996, ISBN 1-56670-200-3 |
| Kemiske egenskaber | Aluminiumfluorid er et hvidt, lugtfrit pulver eller granulat. |
| Kemiske egenskaber | Aluminiumfluorid, AlF3, er et vandfrit krystallinsk pulver med et smeltepunkt på 1291 "C. Aluminiumfluorid (hydratiseret), AlF3·31/2H20, er et hvidt krystallinsk pulver, der er uopløseligt i vand. |
| Bruger | Fremstilling af aluminium for at sænke smeltepunktet og øge elektrolyttens ledningsevne, flux i keramiske glasurer og emaljer, fremstilling af aluminiumsilicat, katalysator. |
| Bruger | Aluminiumfluorid bruges til at fremstille lavtsmeltende aluminiummetal, som flusmiddel i keramiske glasurer og hvide emaljeringer og som katalysator i kemiske reaktioner. |
| Bruger | I keramik, som flusmiddel i metallurgi, i aluminiumfremstilling, som hæmmer af gæring, som katalysator i organiske reaktionerAluminiumfluorid bruges i smelteprocessen til at sænke smeltepunktet for elektrolytter, fremstilling af aluminiumsilikater, raffinering af aluminiumsskrap, produktion af specialitet ildfaste produkter, og i glasindustrien som fyldstof. Det bruges som flusmiddel til at fjerne magnesium. |
| Generel beskrivelse | Lugtfrit hvidt pulver eller granulat. Tættere end vand. Opløselighed i vand ved 25 grader er lig med 0,559 g / 100 ml. |
| Luft- og vandreaktioner | Lidt opløseligt i vand |
| Reaktivitetsprofil | Aluminiumfluorid udsender, når det opvarmes til sublimeringstilstand, giftige fluordampe [USCG, 1999]. |
| Fare | Stærk irriterende for væv. |
| Sundhedsfare | AKUT: luftvejsirritation; mulig næseblødning eller opkastning; KRONISK: forværrer bronkitis/astma; øget knogletæthed. |
| Brandfare | Særlige farer ved forbrændingsprodukter: Udsender giftige fluordampe, når de opvarmes til sublimeringstilstand |
| Antændelighed og eksplosionsevne | Ikke brandfarlig |
| Sikkerhedsprofil | En gift ved indtagelse. Moderat giftig ad subkutan vej. Et stærkt øjenirriterende middel. Voldsomt stødfølsom ved kontakt med Na og K. Ved opvarmning til nedbrydning udsender den giftige dampe af F-. Se også FLUORIDER OG ALUMINIUMSFORBINDELSER. |
| Potentiel eksponering | Anvendes som komponent i elektrolyt, hvorfra aluminiummetal fremstilles; ved fremstilling af keramik, emaljer, aluminiumsilikat; som flux i metallurgi; som fermenteringshæmmer |
| Forsendelse | UN3260 Ætsende fast stof, surt, uorganisk, nej, Fareklasse: 8; Etiketter: 8-Ætsende materiale, teknisk navn påkrævet. UN3077 Miljøfarlige stoffer, fast, nej, Fareklasse: 9; Etiketter: 9-Diverse farlige materialer, teknisk navn påkrævet. |
| Uforeneligheder | Reagerer voldsomt med kalium eller natrium |
| Bortskaffelse af affald | Neutraliser med soda; tilsæt læsket lime; lad stå i 24 timer. Overfør slam til spildevandsanlæg. |
| Aluminiumfluoridpræparationsprodukter og råmaterialer |
| Råvarer | Sulfuric acid-->Sodium carbonate-->Hydrogen fluoride-->Aluminum hydroxide-->Hexafluorosilicic acid-->Calcium fluoride-->PHOS ROCK FERTILIZER IN BULK-->Methylene Blue trihydrate-->Kiselsyre |
| Forberedelsesprodukter | Kaliumfluoroaluminat |
Populære tags: aluminium fluorid, Kina aluminium fluorid producenter, leverandører, fabrik
Du kan også lide
Send forespørgsel


