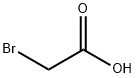
| Kemiske egenskaber |
HVID TIL LYSGUL KRYSTALLINK MASSE |
| Bruger |
Organisk syntese, abscission af citrusfrugter ved høst. |
| Bruger |
Bromeddikesyre bruges i organisk syntese og som alkyleringsmiddel. Det bruges også som et biokemisk stof til proteomikforskning. Det er et vigtigt råmateriale og mellemprodukt, der bruges i organisk syntese, lægemidler, farvestoffer og agrokemikalier. |
| Bruger |
Bromeddikesyre bruges hovedsageligt tilN-terminal bromoacylering af harpiksbundne peptider.
Det kan også bruges:At syntetisere (Z)-2-(cyclooct-4-en-1-yloxy)eddikesyre.
At syntetisere -brom-phenylacetamid.
At omdanne aromatiske thiosemicarbazoner til thiazolylhydrazoner.
|
| Generel beskrivelse |
Vandig opløsning. |
| Luft- og vandreaktioner |
Vandopløselig. |
| Reaktivitetsprofil |
Carboxylsyrer, såsom BROMEDDIKESYRE, donerer hydrogenioner, hvis en base er til stede til at acceptere dem. De reagerer på denne måde med alle baser, både organiske (f.eks. aminerne) og uorganiske. Deres reaktioner med baser, kaldet "neutraliseringer", er ledsaget af udviklingen af betydelige mængder varme. Neutralisering mellem en syre og en base producerer vand plus et salt. Carboxylsyrer med seks eller færre carbonatomer er frit eller moderat opløselige i vand; dem med mere end seks kulstofatomer er lidt opløselige i vand. Opløselig carboxylsyre dissocierer i en grad i vand for at give hydrogenioner. pH-værdien af opløsninger af carboxylsyrer er derfor mindre end 7.0. Mange uopløselige carboxylsyrer reagerer hurtigt med vandige opløsninger indeholdende en kemisk base og opløses, efterhånden som neutraliseringen genererer et opløseligt salt. Carboxylsyrer i vandig opløsning og flydende eller smeltede carboxylsyrer kan reagere med aktive metaller og danne gasformigt brint og et metalsalt. Sådanne reaktioner forekommer i princippet også for faste carboxylsyrer, men er langsomme, hvis den faste syre forbliver tør. Selv "uopløselige" carboxylsyrer kan absorbere nok vand fra luften og opløses tilstrækkeligt i bromeddikesyre til at korrodere eller opløse dele og beholdere af jern, stål og aluminium. Carboxylsyrer, ligesom andre syrer, reagerer med cyanidsalte for at danne gasformigt hydrogencyanid. Reaktionen er langsommere for tørre, faste carboxylsyrer. Uopløselige carboxylsyrer reagerer med opløsninger af cyanider for at forårsage frigivelse af gasformigt hydrogencyanid. Brandfarlige og/eller giftige gasser og varme dannes ved omsætning af carboxylsyrer med diazoforbindelser, dithiocarbamater, isocyanater, mercaptaner, nitrider og sulfider. Carboxylsyrer, især i vandig opløsning, reagerer også med sulfitter, nitritter, thiosulfater (for at give H2S og SO3), dithionitter (SO2), for at generere brændbare og/eller giftige gasser og varme. Deres reaktion med karbonater og bikarbonater genererer en harmløs gas (kuldioxid), men stadig varme. Som andre organiske forbindelser kan carboxylsyrer oxideres af stærke oxidationsmidler og reduceres med stærke reduktionsmidler. Disse reaktioner genererer varme. Et bredt udvalg af produkter er muligt. Som andre syrer kan carboxylsyrer initiere polymerisationsreaktioner; ligesom andre syrer katalyserer de ofte (øger hastigheden af) kemiske reaktioner. |
| Fare |
Stærk irriterende på hud og væv. |
| Sundhedsfare |
GIFTIG; indånding, indtagelse eller kontakt (hud, øjne) med dampe, støv eller stoffer kan forårsage alvorlig skade, forbrændinger eller død. Kontakt med smeltet stof kan forårsage alvorlige forbrændinger på hud og øjne. Reaktion med vand eller fugtig luft vil frigive giftige, ætsende eller brændbare gasser. Reaktion med vand kan generere meget varme, som vil øge koncentrationen af dampe i luften. Brand vil producere irriterende, ætsende og/eller giftige gasser. Afstrømning fra brandkontrol eller fortyndingsvand kan være ætsende og/eller giftigt og forårsage forurening. |
| Brandfare |
Brændbart materiale: kan brænde, men antændes ikke let. Stoffet vil reagere med vand (nogle voldsomt) og frigive brændbare, giftige eller ætsende gasser og afstrømning. Ved opvarmning kan dampe danne eksplosive blandinger med luft: indendørs, udendørs og eksplosionsfare i kloakken. De fleste dampe er tungere end luft. De vil spredes langs jorden og samle sig i lave eller lukkede områder (kloakker, kældre, tanke). Dampe kan bevæge sig til antændelseskilden og blinke tilbage. Kontakt med metaller kan udvikle brændbar brintgas. Beholdere kan eksplodere, når de opvarmes eller forurenes med vand. |
| Antændelighed og eksplosionsevne |
Ikke brandfarlig |
| Sikkerhedsprofil |
Gift ved indtagelse, intraperitoneal og intravenøs vej. Irriterer og ætser hud og slimhinder. Mutationsdata rapporteret. Ved opvarmning til nedbrydning udsender den giftige dampe af Br-. Se også BROMIDER. |
| Oprensningsmetoder |
Krystalliser bromeddikesyre fra pet-ether (b 40-60o). En diethyletheropløsning deraf ledes gennem en aluminiumoxidsøjle, og etheren inddampes ved stuetemperatur under vakuum. Det opnås bedst ved destillation fra en Claisen (kolbe nedsænket i et oliebad) udstyret med en isoleret Vigreux-søjle (s. 11), og fraktionen b 108-110o/30 mm opsamles. Den er lys- og fugtfølsom. [Natelson & Gottfried Org Synth Coll Vol III 381 1955, Beilstein 2 IV 526.] LACHRYMATORY og er hudirriterende. |