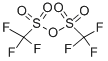
| Beskrivelse |
Trifluormethansulfonsyreanhydrid, også kendt som triflicanhydrid, har vist sig at være et ekstraordinært reagens til en bred vifte af transformationer. Som et kommercielt og let tilgængeligt reagens er det blevet meget brugt i syntetisk kemi på grund af dets høje elektrofilicitet. På grund af dens høje affinitet til O-nukleofiler er reaktion med alkoholer, carbonyler, svovlphosphor- og iodoxider til dannelsen af de tilsvarende triflater stærkt begunstiget. Som en af de førende afgangsgrupper inden for organisk kemi åbner de genererede triflater derefter døren til forskellige nedstrømstransformationer, herunder (men ikke begrænset til) substitutionsreaktioner, krydskoblingsprocesser, redoxreaktioner og omlejringer[1-2] . |
| Kemiske egenskaber |
klar farveløs til lysebrun væske |
| Bruger |
Trifluormethansulfonsyreanhydrid er en stærk elektrofil, der bruges i kemisk syntese til at introducere triflylgruppen. |
| Bruger |
Trifluormethansulfonsyreanhydrid bruges til at omdanne phenoler og imin til triflic-ester og NTf-gruppe. Det er en stærk elektrofil, der bruges til introduktion af triflylgruppe i kemisk syntese. Det tjener som et reagens ved fremstilling af alkyl- og vinyltriflater og til stereoselektiv syntese af mannosazid-methyluronatdonorer. Det fungerer som en katalysator for glycosylering med anomere hydroxysukkere til fremstilling af polysaccharider. |
| Definition |
ChEBI: Triflic anhydrid er et organosulfonsyreanhydrid. Det er funktionelt relateret til en triflinsyre. |
| Reaktivitetsprofil |
Elektrofil aktivering af tertiære og sekundære amider med triflinsyreanhydrid (Tf2O; rifluormethansulfonsyreanhydrid) under milde forhold giver anledning til henholdsvis iminium- og iminotriflater, som kunne bruges som alsidige reagenser til at reagere med forskellige C-, N-, O- og S -nukleofiler til transformation af en amidfunktion til forskellige produkter. Andre oxygenholdige nukleofiler, såsom sulfoxider og phosphoroxider, kunne også gennemgå nukleofilt angreb med Tf2O for at generere thioniumtriflat, elektrofile P-arter og phosphoniumtriflat. Disse meget aktive forbigående arter kunne let gennemgå nukleofile substitutionsreaktioner for yderligere forskellige transformationer. På grund af den stærke elektrofile egenskab er Tf2O desuden tilbøjelig til at reagere med relativt svage nukleofiler, såsom nitrilgrupper eller nogle nitrogenholdige heterocykliske forbindelser. Derudover er Tf2O også blevet brugt som en effektiv radikal trifluormethylerings- og trifluormethylthioleringsreagens gennem frigivelse af SO2 eller deoxygeneringsproces til syntese af trifluormethylerede og trifluormethylthiolerede forbindelser[2]. |
| Fare |
Kan være ætsende for metaller. Farlig ved indtagelse. Forårsager alvorlige forbrændinger af huden og øjenskader. |
| Antændelighed og eksplosionsevne |
Ikke klassificeret |
| Syntese |
Syntesen af trifluormethansulfonsyreanhydrid er som følger:
En tør, {0}}ml., rundbundet kolbe fyldes med 36,3 g. (0,242 mol) trifluormethansulfonsyre (note 1) og 27,3 g. (0,192 mol) phosphorpentoxid (note 2). Kolben tilproppes og får lov at stå ved stuetemperatur i mindst 3 timer. I løbet af denne periode ændres reaktionsblandingen fra en opslæmning til en fast masse. Kolben er forsynet med et kortvejsdestillationshoved og opvarmes først med en strøm af varm luft fra en varmepistol og derefter med flammen fra en lille brænder.Kolben opvarmes, indtil der ikke længere destillerer trifluormethansulfonsyreanhydrid, kogepunkt 82-115 grader, hvilket giver 28,4-31,2 g. (83-91%) af anhydridet, en farveløs væske. Selvom dette produkt er tilstrækkeligt rent til brug i det næste trin, kan den resterende syre fjernes fra anhydridet ved følgende procedure. En opslæmning på 3,2 g. phosphorpentoxid i 31,2 g. af det rå anhydrid omrøres ved stuetemperatur i en proppet kolbe i 18 timer. Efter at reaktionskolben er blevet udstyret med et kortvejsdestillationshoved, opvarmes den med et oliebad, hvilket giver 0,7 g. af forløb, bp 74-81 grader, efterfulgt af 27,9 g. af det rene trifluormethansulfonsyreanhydrid, kogepunkt 81-84 grader.

|
| opbevaring |
Opbevares på et køligt, tørt, godt ventileret område. Fugt følsom. |
| Oprensningsmetoder |
Det kan friskfremstilles ud fra den vandfri syre (11,5 g) og P2O5 (11,5 g, eller halvdelen af denne vægt) ved at stille det til side ved stuetemperatur i 1 time, destillere flygtige produkter af og destillere det derefter gennem en kort Vigreux-søjle. Det hydrolyseres let af H2O og nedbrydes betydeligt efter et par dage for at frigive SO2 og producere en viskøs væske. Opbevar det tørt ved lave temperaturer. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Referencer |
[1] Haoqi Zhang. "Trifluormethansulfonsyreanhydrid i amidaktivering: Et kraftfuldt værktøj til at skabe heterocykliske kerner." TCIMAIL (2021).
[2] Dr. Qixue Qin, Prof. Dr. Ning Jiao, Zengrui Cheng. "Nylige anvendelser af trifluormethansulfonsyreanhydrid i organisk syntese." Angewandte Chemie 135 10 (2022). |