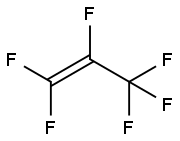
| Kemiske egenskaber |
Hexafluorpropylen (HFP) er en farveløs, lugtfri, ikke-brændbar gas, der kun er lidt opløselig i vand. Det bruges som kemisk mellemprodukt primært i syntesen af fluorpolymerer, fluorelastomerer og fluorerede materialer (f.eks. funktionelle perfluorpolyethervæsker, olier og fedtstoffer). |
| Bruger |
Hexafluorpropen bruges i syntesen af polyvinylidenfluorid-co-hexafluorpropylen, en polymer, som i øjeblikket bruges i forskellige områder af nano- og elektroniske sektorer lige fra membraner til nanopartikler. |
| Forberedelse |
Hexafluorpropylen kan fremstilles ved pyrolyse af tetrafluorethylen (TFE):
3 CF2=CF2 → 2 CF3CF=CF
Denne reaktion udføres i en lukket kontinuerlig reaktor ved 600 til 900 grader. Udbyttet kan forbedres ved lavt partialtryk, opnået enten ved at arbejde under reduceret totaltryk (ned til 0,1 bar) eller ved at indsprøjte et inert fortyndingsmiddel såsom damp eller CO2.
Betydelige mængder af biprodukter, herunder den meget giftige perfluorisobutylen (PFIB), dannes under pyrolysen af TFE. Sådanne biprodukter forbrændes enten direkte eller indsamles og transporteres til forbrænding på et fjerntliggende anlæg.
Hexafluorpropylen kan også fremstilles ud fra chlordifluormethan eller fremstilles af forskellige chlorfluorcarboner. |
| Syntesereference(r) |
Journal of the American Chemical Society, 73, s. 4054, 1951DOI:10.1021/ja01152a548 |
| Generel beskrivelse |
Hexafluorpropylen er en lugtfri, farveløs gas. Hexafluorpropylen er ikke-brændbart. Hexafluorpropylen kan kvæle ved fortrængning af luft. Udsættelse af beholderen for langvarig varme eller ild kan få hexafluorpropylen til at briste voldsomt og eksplodere. |
| Reaktivitetsprofil |
Halogenerede alifatiske forbindelser, såsom hexafluorpropylen, er moderat eller meget reaktive. Reaktiviteten falder generelt med øget grad af substitution af halogen til hydrogenatomer. Materialer i denne gruppe kan være uforenelige med stærke oxidations- og reduktionsmidler. De kan også være uforenelige med mange aminer, nitrider, azo/diazoforbindelser, alkalimetaller og epoxider. Over et minimum oxygentryk bliver reaktionen af oxygendifluorid og hexafluorpropen for at give hexafluorpropylenoxidet eksplosiv, Chem. Abs., 1987, 107, 175302. Reaktionen af hexafluorpropen med grignardreagens (subst. phenylmagnesiumbromider) førte til eksplosion, Fluorine Chem., 1981, 18, 25. |
| Sundhedsfare |
Dampe kan uden varsel forårsage svimmelhed eller kvælning. Dampe fra flydende gas er i starten tungere end luft og spredes langs jorden. Kontakt med gas eller flydende gas kan forårsage forbrændinger, alvorlige kvæstelser og/eller forfrysninger. Brand kan producere irriterende, ætsende og/eller giftige gasser. |
| Brandfare |
Nogle kan brænde, men ingen antændes let. Beholdere kan eksplodere ved opvarmning. Sprængte cylindre kan eksplodere. |
| Antændelighed og eksplosionsevne |
Ikke brandfarlig |