
Produkt introduktion
| Pyridin Grundlæggende information |
| Kemisk struktur Kemiske egenskaber Produktioner Anvendelser Toksicitetsoplysninger Farer Referencer |
| Produktnavn: | Pyridin |
| Synonymer: | pyridincarboxylsyre,2-(4,5-dihydro-4-methyl-4-(1-methylethyl)-5-oxo-1h-imidazol{ {9}}yl)-5-methyl;pyridincarboxylsyre,2-(4,5-dihydro-4-methyl-4-(1-methylethyl){{ 17}}oxo-1h-imidazol-2-yl)-5-methyl,monoammoniumsalt;Rcra affaldsnummer U196;rcrawastenumberu196;FEMA 2932;FEMA 2966;FEMA NUMMER 2966;azabenzen |
| CAS: | 110-86-1 |
| MF: | C5H5N |
| MW: | 79.1 |
| Einecs: | 203-809-9 |
| Produktkategorier: | Ravfarvede glasflasker;NMR;Opløsningsmiddelflasker;Opløsningsmiddel efter anvendelse;Opløsningsmiddel efter type;Opløsningsmiddelemballagemuligheder;Bioteknologiske opløsningsmidlerOpløsningsmidler;Opløsningsmiddelflasker;Opløsningsmidler;Sikker/forsegling? Flasker; Spektrofotometrisk kvalitet; Spektrofotometriske opløsningsmidler; Spektroskopi opløsningsmidler (IR; UV/Vis); Organostannes; Tributylstanny; Kemi; PS; Alpha Sort; Flygtige stoffer/ Halvflygtige stoffer; Ravglasflasker; ReagensPlus(R) Opløsningsmiddel Plu-produkter (R) Reagens-kvalitetsprodukter; ;ACS Grade Solvents;CHROMASOLV PlusCHROMASOLV Solvents (HPLC, LC-MS);CHROMASOLV(R) Plus;LC-MS Plus and Gradient;Alphabetic;P;PU - PZ;Pyridin;Organohalides;Boronic ester;Organoborons;Organosilane;ACS Grade -Bulkopløsningsmidler;ACS-kvalitetsopløsningsmidler;kulstofståldåser med NPT-gevind;Returbare beholderopløsningsmidler;ACS- og reagenskvalitetsopløsningsmidler;ReagentPlus;ReagentPlus-produkter af opløsningsmiddelkvalitet;Bioteknologiske opløsningsmidler;Sure/forsegle flasker;ACS-kvalitet;Analytiske reagenser til generel brug; ;Analytisk/kromatografi;Multi-kompendiel;Puriss pa;Puriss pa ACS;PVC-belagte flasker;aluminiumsflasker;CHROMASOLV Plus;Chromatography Reagents &;HPLC &;HPLC Plus Grade Solvents (CHROMASOLV);HPLC/UHPLC Solvents (UPVCHLCOLvents); Opløsningsmidler (CHROMASOLV);ACS-opløsningsmidler;Carbonståldåser med NPT-gevind;Semi-Bulk opløsningsmidler;Halogenerede;Fluorerede;Byggesten;Borsyre;Carboxy;Alkoxy;Analytiske reagenser til generel brug;OP, Puriss pa;Puriss pa;OP , Puriss pa ACS;Puriss pa ACS;Aluminiumsflasker;Alfabetiske lister;Smagsstoffer og dufte;OP;Spektrofotometrisk Grade Solvents;Spectrophotometric GradeSolvents;PVC Coated Bottles;ReagentPlus(R) Solvent Grade ProductsSolvents;VanfriSolvents{0}Opløsningsmidler{0; };bc0001 |
| Mol fil: | 110-86-1.mol |
 |
|
| Pyridin kemiske egenskaber |
| Smeltepunkt | -42 grad (belyst) |
| Kogepunkt | 115 grader (belyst) |
| massefylde | 0.978 g/ml ved 25 grader (lit.) |
| damptæthed | 2,72 (i forhold til luft) |
| Damptryk | 23,8 mm Hg (25 grader) |
| brydningsindeks | n20/D 1.509 (lit.) |
| FEMA | 2966|PYRIDIN |
| Fp | 68 grader F |
| opbevarings temp. | Opbevar ved +5 grader til +30 grader . |
| opløselighed | H2O: i overensstemmelse |
| PKA | 5,25 (ved 25 grader) |
| formular | Væske |
| farve | farveløs |
| Lugt | Kvalmende lugt registreres ved 0.23 til 1.9 ppm (gennemsnitlig=0.66 ppm) |
| Relativ polaritet | 0.302 |
| PH | 8,81 (H2O, 20 grader) |
| eksplosionsgrænse | 12.4% |
| Lugttærskel | 0.063 sider/min |
| Lugttype | fiskeagtig |
| Vandopløselighed | Blandbar |
| Frysepunkt | -42 grad |
| λmax | λ: 305 nm Amax: 1.00 λ: 315 nm Amax: 0.15 λ: 335 nm Amax: 0,02 λ: {{0}} nm Amax: 0,01 |
| Merck | 14,7970 |
| BRN | 103233 |
| Henrys lovkonstant | 18,4 ved 30 grader (headspace-GC, Chaintreau et al., 1995) |
| Eksponeringsgrænser | TLV-TWA 5 ppm (-15 mg/m3) (ACGIH, MSHA og OSHA); STEL 10 ppm (ACGIH), IDLH 3600 ppm (NIOSH). |
| Dielektrisk konstant | 12,5 (20 grader) |
| Stabilitet: | Stabil. Brandfarlig. Uforeneligt med stærke oxidationsmidler, stærke syrer. |
| InChIKey | JUJWROOIHBZHMG-UHFFFAOYSA-N |
| LogP | 0.64 ved 20 grader |
| CAS Database Reference | 110-86-1(CAS DataBase Reference) |
| NIST Kemi Reference | Pyridin(110-86-1) |
| IARC | 2B (Vol. 77, 119) 2019 |
| EPA stofregistreringssystem | Pyridin (110-86-1) |
| Sikkerhedsoplysninger |
| Farekoder | T,N,F,Xn |
| Risikoerklæringer | 11-20/21/22-39/23/24/25-23/24/25-52-36/38 |
| Sikkerhedserklæringer | 36/37/39-38-45-61-28A-26-28-24/25-22-36/37-16-7 |
| OEB | A |
| OEL | TWA: 5 ppm (15 mg/m3) |
| RIDADR | UN 1282 3/PG 2 |
| WGK Tyskland | 2 |
| RTECS | UR8400000 |
| F | 3-10 |
| Selvantændelsestemperatur | 482 grader |
| Farebemærkning | Meget brandfarlig/skadelig |
| TSCA | Ja |
| HS kode | 2933 31 00 |
| Fareklasse | 3 |
| Pakkegruppe | II |
| Data om farlige stoffer | 110-86-1(data om farlige stoffer) |
| Toksicitet | LD50 oralt hos rotter: 1,58 g/kg (Smyth) |
| IDLA | 1,000 ppm |
| MSDS-oplysninger |
| Udbyder | Sprog |
|---|---|
| Sigma Aldrich | engelsk |
| ACROS | engelsk |
| ALFA | engelsk |
| Pyridinbrug og syntese |
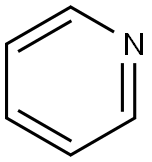
| Kemisk struktur | Pyridin er en basisk heterocyklisk organisk forbindelse med den kemiske formel C5H5N. Det er strukturelt beslægtet med benzen, med en methingruppe (=CH−) erstattet af et nitrogenatom. Pyridinringen forekommer i mange vigtige forbindelser, herunder aziner og vitaminerne niacin og pyridoxin.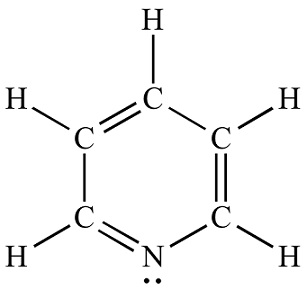 Pyridine Lewis struktur |
| Kemiske egenskaber | Pyridin er en farveløs brændbar væske med en stærk og ubehagelig fiskelignende lugt. Pyridin |
| Produktioner | 2.1 Adskillelse fra tjære Pyridinbaser er en bestanddel af tjære. De blev isoleret fra stenkulstjære eller kulgas, før syntetiske fremstillingsprocesser blev etableret. Mængderne indeholdt i stenkulstjære og kulgas er små, og pyridinbaserne isoleret fra dem er en blanding af mange komponenter. Således, med nogle få undtagelser, var isolering af rene pyridinbaser dyr. I dag produceres næsten alle pyridinbaser ved syntese.2.2 Chichibabin syntese 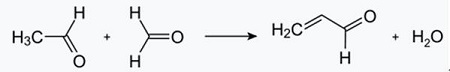 Fig. 2-1Dannelse af acrolein ud fra acetaldehyd og formaldehyd 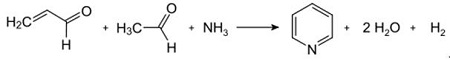 Fig. 2-2Kondensation af pyridin fra acrolein og acetaldehyd Chichibabin-pyridinsyntesen blev rapporteret i 1924 og er stadig i brug i industrien. Acetaldehyd og formaldehyd reagerer med ammoniak og giver hovedsageligt pyridin. Først dannes acrolein i en Knoevenagel-kondensation fra acetaldehydet og formaldehydet. Det kondenseres derefter med acetaldehyd og ammoniak til dihydropyridin og oxideres derefter med en faststofkatalysator til pyridin. Reaktionen udføres sædvanligvis ved 350-550°C og en rumhastighed på 500-1000 timer-1i nærvær af en fast syrekatalysator (f.eks. silica-aluminiumoxid). Produktet består af en blanding af pyridin, simple methylerede pyridiner (picolin) og lutidin. Den genvundne pyridin adskilles fra biprodukter i en flertrinsproces. 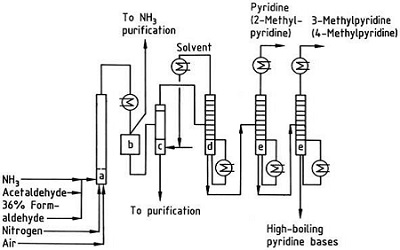 Fig. 2-3Flowskema over pyridin- og methylpyridinproduktion fra acetaldehyd og formaldehyd med ammoniak. A) Reaktor; b) Samler; c) Ekstraktion; d) opløsningsmiddeldestillation; e) Destillation 2.3 Dealkylering af alkylpyridiner Pyridin kan fremstilles ved dealkylering af alkylerede pyridiner, som opnås som biprodukter i syntesen af andre pyridiner. Den oxidative dealkylering udføres enten ved anvendelse af luft over vanadium(V)oxidkatalysator, ved dampdealkylering på nikkelbaseret katalysator eller hydrodealkylering med en sølv- eller platinbaseret katalysator. Udbytter af pyridin på op til 93% kan opnås med den nikkelbaserede katalysator. 2.4 Syntese fra nitriler og acetylen Væskefasereaktion af nitriler med acetylen udføres ved 120-180 ?C og 0.8-2.5 MPa i nærværelse af en organokoboltkatalysator og giver 2-substituerede pyridiner : 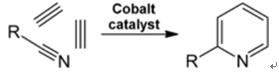 Fig. 2-4Syntese af 2-methylpyridin fra nitriler og acetylen Trimeriseringen af en del af et nitrilmolekyle og to dele acetylen til pyridin kaldes Bönnemann-cyklisering. Ved anvendelse af acetonitril som nitril opnås 2-methylpyridin, som kan dealkyleres til pyridin. 2.5 Syntese fra acrylonitril og ketoner 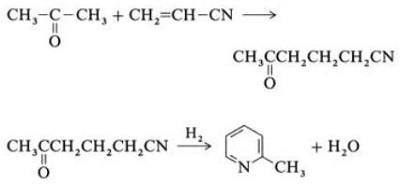 Fig. 2-5Syntese af 2-methylpyridin fra acrylonitril og acetone Syntese fra acrylonitril og acetone giver 2-methylpyridin selektivt, som kan dealkyleres til pyridin. For det første sker reaktionen af acrylonitril og acetone, katalyseret af en primær alifatisk amin såsom isopropylamin og en svag syre såsom benzoesyre, i væskefasen ved 180 °C og 2,2 MPa for at give 5-oxohexanenitril med 91 % selektivitet. Acrylnitril-omdannelsen er 86%. Derefter udføres ringslutning og dehydrering af det oprindelige produkt i gasfasen i nærvær af hydrogen over en palladium-, nikkel- eller cobaltholdig katalysator ved 240°C for at give 2-methylpyridin i 84 % udbytte. 2.6 Syntese fra dinitriler I en dampfasereaktion over en nikkelholdig katalysator i nærværelse af hydrogen giver 2-methylglutaronitril 3-methylpiperidin, som derefter undergår dehydrogenering over palladium-aluminiumoxid for at give 3-methylpyridin. Og 3-methylpyridin kan også dealkyleres til pyridin. 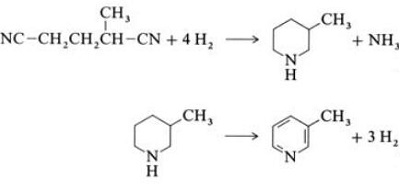 Fig. 2-6Syntese af 2-methylpyridin fra dinitriler En et-trins gasfasereaktion over en palladiumholdig katalysator rapporteres at give 3-methylpyridin i 50 % udbytte. 2.7 Biosyntese Adskillige pyridinderivater spiller vigtige roller i biologiske systemer. Mens biosyntesen ikke er fuldt ud forstået, forekommer nikotinsyre (vitamin B3) i nogle bakterier, svampe og pattedyr. Pattedyr syntetiserer nikotinsyre gennem oxidation af aminosyren tryptofan, hvor et mellemprodukt, anilin, danner et pyridinderivat, kynurenin. Tværtimod producerer bakterierne Mycobacterium tuberculosis og Escherichia coli nikotinsyre ved kondensering af glyceraldehyd-3-phosphat og asparaginsyre. 2.8 Andre metoder Ethylen og ammoniak reagerer i nærværelse af en palladiumkomplekskatalysator for at give 2-methylpyridin og MEP. Pyridin kan fremstilles ud fra cyclopentadien ved ammoxidation eller ud fra 2-pentennitril ved ringslutning og dehydrogenering. Furfurylalkohol eller furfural reagerer med ammoniak i gasfasen og giver pyridin. 2-Methylpyridin fremstilles også ud fra anilin. |
| Bruger | 3.1 Opløsningsmiddel Pyridin(110-86-1) er et polært, basisk, lavreaktivt opløsningsmiddel, især til dehydrochloreringsreaktioner og ekstraktion af antibiotika. I eliminationsreaktionen fungerer pyridin som basis for eliminationsreaktionen og binder det resulterende hydrogenhalogenid til dannelse af et pyridiniumsalt. Ved esterificeringer og acyleringer aktiverer pyridin carboxylsyrehalogeniderne eller anhydriderne. 3.2 Medicin Pyridins kemiske struktur kan findes i forskellige medikamenter, der syntetiseres til dels takket være pyridin. Et eksempel er en medicin kaldet esomeprazol, det generiske navn for Nexium. Dette er en medicin, der bruges til at behandle GERD eller gastroøsofageal reflukssygdom. Et andet eksempel på en pyridinholdig medicin er loratadin, mere almindeligt kendt under sit varemærke Claritin. Loratadin hjælper i behandlingen af allergier. 3.3 Pesticider Hovedanvendelsen af pyridin er som forløber for herbiciderne paraquat og diquat. Det første syntesetrin af insekticidet chlorpyrifos består af chlorering af pyridin. Pyridin er også udgangsforbindelsen til fremstilling af pyrithion-baserede fungicider. Cetylpyridinium og laurylpyridinium, som kan fremstilles af pyridin med en Zincke-reaktion, bruges som antiseptisk i mund- og tandplejeprodukter. Pyridin angribes let af alkyleringsmidler for at give N-alkylpyridiniumsalte. Et eksempel er cetylpyridiniumchlorid.  Fig 3-1 Syntese af paraquat 3.4 Syntese af piperidin Piperidin, en fundamental nitrogen-heterocyklus, er en vigtig syntetisk byggesten. Piperidiner fremstilles ved hydrogenering af pyridin med en nikkel-, cobalt- eller ruthenium-baseret katalysator ved forhøjede temperaturer. C5H5N + 3 H2 → C5H10NH3,5 Ligand og Lewis-base Pyridin er meget udbredt som en ligand i koordinationskemi. Som en ligand af metalkompleks kan den let erstattes af en stærkere Lewis-base, som kan bruges i katalyse af polymerisations- og hydrogeneringsreaktioner. Efter afslutningen af reaktionen kan pyridinligand erstattet under reaktionen genoprettes igen. Pyridin bruges også som base i kondensationsreaktioner. Som base kan pyridin bruges som Karl Fischer-reagenset, men det erstattes normalt af alternativer med en mere behagelig lugt, såsom imidazol. 3.6 Andre Bortset fra ovennævnte anvendelser, bruges Pyridine også til at fremstille polycarbonatharpikser, vitaminer, fødevarearomaer, maling, farvestoffer, gummiprodukter, klæbemidler og vandtætning til stoffer. Pyridin tilsættes ethanol for at gøre det uegnet til at drikke. Det bruges også til in vitro-syntese af DNA. |
| Toksicitetsoplysninger | 4.1 Toksicitetsniveau Lav toksicitet 4.2 Akut toksicitet LD501580mg/kg (store mus, oral); 1121mg/kg (kanin, gennem huden); indåndes af mennesker 25mg/m3×20 min, irritation af bindehinde og øvre luftvejsslimhinde. Subakut og kronisk toksicitet: inhaleret af store mus 32,3mg/m3×7 timer/dag x5 dage/uge x6 måneder, stigning i levervægt; indåndes af mennesker 20-40mg/m3 (langsigtet), nerveskade, ustabil gang, digitale rystelser, lavt blodtryk, oversvedning, lejlighedsvis lever- og nyreskade. |
| Farer | 5.1 Sundhedsfarer Pyridin er ekstremt giftigt ved indtagelse og indånding. Dampe er tungere end luft. dens forbrænding producerer giftige nitrogenoxider. Pyridin er meget brandfarligt (dets flammepunkt er kun 17 ºC). Pyridin kan også have neurotoksiske og genotoksiske virkninger. 5.2 Brandfarer Opførsel i brand: Damp er tungere end luft og kan rejse betydelige afstande til antændelseskilden og flash back. |
| Referencer |
https://en.wikipedia.org/wiki/Pyridin#Occurrence http://www.zwbk.org/MyLemmaShow.aspx?zh=zh-tw&lid=169038 http://www.softschools.com/formulas/chemistry/pyridine_formula/378/ http://www.hmdb.ca/metabolites/HMDB0000926 https://study.com/academy/lesson/pyridine-in-medicine-uses-synthesis.html#partialRegFormModal http://www.toxipedia.org/display/toxipedia/Pyridin https://www.chemicalbook.com/ProductChemicalPropertiesCB8852825_DA.htm https://pubchem.ncbi.nlm.nih.gov/compound/pyridin#section=Top http://www.ebi.ac.uk/chebi/searchId.do;jsessionid=E7088896622D62FC650863C2AD197CAA?chebiId=CHEBI:16227 https://www.britannica.com/science/pyridin Shimizu, S.; Watanabe, N.; Kataoka, T.; Shoji, T.; Abe, N.; Morishita, S.; Ichimura, H. (2005), "Pyridine and Pyridine Derivatives", Ullmanns Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_399 |
| Kemiske egenskaber | Pyridin, er en let gul eller farveløs væske; hygroskopisk; ubehagelig lugt; brændende smag; svagt alkalisk i reaktion; opløselig i vand, alkohol, ether, benzen og fede olier; specifik vægtfylde, 0.978; selvantændelsestemperatur, 482 grader. Pyridin, en tertiær amin, er en noget stærkere base end anilin og danner let kvaternære ammoniumsalte. |
| Kemiske egenskaber | Pyridin er en svag base (pKa{{0}}.25); en 0,2 M opløsning har en pH på 8,5 (HSDB 1988). Dets carbonatomer deaktiveres mod elektrofil substitution. Dette gælder især i sure medier, hvor der dannes salte ved nitrogenet. Det undergår imidlertid let nukleofil substitution, fortrinsvis ved C-2 og også i C-4-positionen (Jori et al. 1983). Da pyridin er en tertiær amin, reagerer pyridin med alkyleringsmidler til dannelse af kvaternære salte (Santodonato et al. 1985). På grund af dens reducerede kapacitet til at donere elektroner er den mere modstandsdygtig over for oxidation end benzen. Oxidation med peroxysyrer danner pyridin-N-oxid, som derefter er i stand til at undergå elektrofil substitution (Jori et al 1983). Pyridin reagerer voldsomt med en række forbindelser, herunder salpetersyre, svovlsyre, maleinsyreanhydrid, perchromat, beta-propiolacton og chlorsulfonsyre. Termisk nedbrydning kan frigive cyanider (Gehring 1983). Både pyridiniumionen og pyridinen i sig selv reduceres let til den kommercielt vigtige forbindelse, piperidin (Jori et al. 1983). |
| Fysiske egenskaber | Klar, farveløs til bleggul, brændbar væske med en skarp, gennemtrængende, kvalmende fiskelignende lugt. Lugttærskelkoncentrationer i vand og luft var 2 ppm (Buttery et al., 1988) og 21 ppbv(Leonardos et al., 1969). Detektion af lugtgrænsekoncentrationer på 0,74 mg/m3(2,3 ppmv) og 6 mg/m3(1,9 ppmv) blev eksperimentelt bestemt af henholdsvis Katz og Talbert (1930) og Dravnieks (1974). Cometto-Mu?iz og Cain (1990) rapporterede en gennemsnitlig tærskelkoncentration for nasal skarphed på 1.275 ppmv. |
| Hændelse | Pyridin blev opdaget af Anderson i stenkulstjære i 1846 (Windholz et al. 1983). Det findes i tobaksrøg (Vohl og Eulenberg 1871; Lehmann 1909) og brændt kaffe (Bertrand og Weisweiller 1913). Pyridin findes i træolie og i blade og rødder af Atropa belladonna (HSDB 1988), og er også en bestanddel af creosotolie (Krone et al 1986). I naturen findes pyridin og dets derivater almindeligvis som komponenter af alkaloider, vitaminer og coenzymer. |
| Bruger | Pyridin bruges som opløsningsmiddel i maling- og gummiindustrien; som mellemprodukt i farvestoffer og lægemidler; til denaturering af alkohol; og som reagens til cyanidanalyse. Det forekommer i stenkulstjære. |
| Bruger | Pyridin anvendes direkte ved denaturering af alkohol (ACGIH 1986; HSDB 1989; NSC 1978) og som opløsningsmiddel i maling og gummipræparat (ACGIH 1986; HSDB 1989; NSC 1978) og i forskningslaboratorier til funktioner som udvinding af plantehormoner ( Santodonato et al. 1985). Halvdelen af den pyridin, der produceres i dag, bruges som mellemprodukt til fremstilling af forskellige insekticider og herbicider til landbrugsanvendelser (ACGIH 1986; Harper et al. 1985; Santodonato et al. 1985). Cirka 20 % går til produktionen af piperidin (Harper et al. 1985; Santodonato et al. 1985), som er kommercielt betydningsfuldt i fremstillingen af kemikalier, der anvendes til gummivulkanisering og landbrug (NSC 1978). Pyridin bruges også som et mellemprodukt i fremstillingen af lægemidler (antihistaminer, steroider, sulfa-type og andre antibakterielle midler), farvestoffer, vandafvisende midler og polycarbonatharpikser (ACGIH 1986; Harper et al. 1985; NSC 1978; Santodonato et al. 1985). Pyridin er også godkendt af Food and Drug Administration (FDA) til brug som et smagsstof ved tilberedning af fødevarer (Harper et al. 1985; HSDB 1989). |
| Definition | ChEBI: Pyridin er en azaaren, der omfatter en benzenkerne, hvor en -CH-gruppe er erstattet af et nitrogenatom. Det er moderforbindelsen til klassen pyridiner. Molekylerne har en hexagonal plan ring og er isoelektroniske med benzen. Pyridin er et eksempel på en aromatisk heterocyklisk forbindelse, hvor elektronerne i carbon-carbon pi-bindingerne og det enlige par af nitrogen er delokaliseret over atomringen. Forbindelsen udvindes af stenkulstjære og anvendes som opløsningsmiddel og som råmateriale til organisk syntese. |
| Produktionsmetoder | Pyridin fremstilles af gasser opnået ved koksning af kul og ved direkte syntese. Den lette oliefraktion af stenkulstjære behandles med svovlsyre til fremstilling af vandopløselige pyridinsalte, og derefter genvindes pyridinbaserne fra den vandige fase med natriumhydroxid eller ammoniak (Jori et al. 1983). Størstedelen af amerikansk produktion sker gennem syntetiske midler. Denne proces anvender en dampfasereaktion af acetaldehyd, formaldehyd og ammoniak, som giver en blanding af pyridin og 3-methylpyridin (Santodonato et al 1985). Produktforholdet afhænger af de relative mængder af acetaldehyd og formaldehyd. Tilsat methanol øger udbyttet. Den amerikanske produktion af pyridin blev anslået til 32 til 47 millioner pund i 1975 (Reinhardt og Brittelli 1981). Pyridin er kommercielt tilgængelig i tekniske, 2 graders og 1 graders kvaliteter, de to sidstnævnte refererer til deres kogeintervaller. Større urenheder er højerekogende homologer, såsom picoliner, lutidiner og collidiner, som er mono-, di- og trimethylpyridiner (Santodonato et al 1985; Jori et al 1983). |
| Forberedelse | Pyridin fremstilles enten ved isolering fra naturlige kilder såsom kul eller gennem kemisk syntese (HSDB 1989). Pyridin fremstilles ved fraktioneret destillation af stenkulstjærerester (HSDB 1989; NSC 1978; Santodonato et al. 1985), hvor 1 ton kul producerer 0.07-0.21 pounds pyridinbaser af hvor 57 % er pyridin (Santodonato et al., 1985). Syntetisk fremstillet pyridin er i øjeblikket den vigtigste kilde til pyridin til kommerciel anvendelse (Santodonato et al. 1985). Små mængder pyridin syntetiseres fra acetaldehyd, formaldehyd og ammoniak med en fluidiseret silica-aluminiumoxid-katalysator, efterfulgt af fraktionering for at isolere pyridinen (Harper et al. 1985; HSDB 1989; NSC 1978). Pyridin fremstilles fra naturlige kilder af Crowley Tar Products fra Stow, Ohio og Oklahoma City, Oklahoma (Harper et al. 1985; HSDB 1989; SRI 1986, 1987, 1988). Pyridin fremstilles syntetisk af to virksomheder, Nepera Chemical Co. i Harriman, New York og Reilly Tar and Chemical Corporation i Indianapolis, Indiana (Harper et al. 1985; SRI 1986, 1987, 1988). |
| Aroma tærskelværdier | Registrering: 0.079 til 790 ppb; genkendelse: 7,9 til 40 ppm |
| Generel beskrivelse | En klar farveløs til lysegul væske med en gennemtrængende kvalmende lugt. Massefylde 0.978 g/cm3. Flammepunkt 68 grader F. Dampe er tungere end luft. Giftig ved indtagelse og indånding. Forbrænding producerer giftige oxider af nitrogen. |
| Luft- og vandreaktioner | Meget brandfarlig. Opløseligt i vand. |
| Reaktivitetsprofil | Azabenzen er en base. Reagerer eksotermt med syrer. Under fremstilling af et kompleks af azabenzen med chromtrioxid, en syre, blev andelen af chromtrioxid øget. Opvarmning fra denne syre-base reaktion førte til en eksplosion og brand [MCA Case History 1284 1967]. En 0,1 % opløsning af azabenzen (eller anden tertiær amin) i maleinsyreanhydrid ved 185 grader giver en eksoterm nedbrydning med hurtig udvikling af gas [Chem Eng. Nyheder 42(8); 41 1964]. Blanding af azabenzen i lige molære portioner med et af følgende stoffer i en lukket beholder fik temperaturen og trykket til at stige: chlorsulfonsyre, salpetersyre (70%), oleum, svovlsyre (96%) eller propiolacton [NFPA 1991]. Kombinationen af jod, azabenzen, svovltrioxid og formamid udviklede en gas over tryk efter flere måneder. Dette opstod fra den langsomme dannelse af svovlsyre fra eksternt vand eller fra dehydrering af formamidet til hydrogencyanid. Ethylenoxid og SO2 kan reagere voldsomt i azabenzenopløsning med tryk, hvis ethylenoxid er i overskud (Nolan, 1983, Case History 51). |
| Fare | Brandfarlig, farlig brandrisiko, eksplosionsgrænser i luft 1,8–12,4 %. Giftig ved indtagelse og indånding. Hudirriterende, lever- og nyreskader. Tvivlsomt kræftfremkaldende. |
| Sundhedsfare | Den akutte toksicitet af pyridin er lav. Indånding forårsager irritation af luftvejene og kan påvirke centralnervesystemet og forårsage hovedpine, kvalme, opkastning, svimmelhed og nervøsitet. Pyridin irriterer øjne og hud og absorberes let, hvilket fører til systemiske effekter. Indtagelse af pyridin kan resultere i lever- og nyreskader. Pyridin forårsager lugttræthed, og dets lugt giver ikke tilstrækkelig advarsel om tilstedeværelsen af skadelige koncentrationer. Pyridin har ikke vist sig at være kræftfremkaldende eller at vise reproduktions- eller udviklingstoksicitet hos mennesker. Kronisk eksponering for pyridin kan resultere i skader på leveren, nyrerne og centralnervesystemet. |
| Sundhedsfare | De toksiske virkninger af pyridin omfatter hovedpine, svimmelhed, nervøsitet, kvalme, søvnløshed, hyppig vandladning og mavesmerter. Symptomerne var forbigående, forekom hos mennesker fra subakut eksponering for pyridindampe ved ca. 125 ppm i 4 timer om dagen i 1-2 uger (Reinhardt) og Brittelli 1981). Målorganerne for pyridintoksicitet er centralnervesystemet, leveren, nyrerne, mave-tarmkanalen og hud. Eksponeringsvejene er indånding af dampe og indtagelse og absorption af væsken gennem huden. Alvorlige sundhedsfarer kan opstå ved kronisk indånding, som kan forårsage nyre- og leverskader, og stimulering af knoglemarv for at øge produktionen af blodplader. Lavt niveau eksponering for 10 ppm kan give kroniske forgiftningseffekter på centralnervesystemet. Indtagelse af væsken kan give de samme symptomer som ovenfor nævnt. Hudkontakt kan forårsage dermatitis. Damp er irriterende for øjne, næse og lunger. På grund af dens stærke ubehagelige lugt er der altid tilstrækkelig advarsel mod enhver overeksponering. En koncentration på 10 ppm er upassende for mennesker. LCLO værdi, indånding (rotter): 4000 ppm/4 timer LD50-værdi, oral (mus): 1500 mg/kg. Huh og kolleger (1986) har undersøgt effekten af glycyrrhetinsyre på pyridintoksicitet hos mus. Forbehandling med glycyrrhetinsyre reducerede undertrykkelse af centralnervesystemet og dødelighed hos dyr induceret af pyridin. En sådan forbehandling reducerede markant aktiviteten af enzymet serumtransaminase og øgede aktiviteten af hepaticmikrosomal anilinhydroxylase [9012-90-0], et pyridinmetaboliserende enzym. |
| Antændelighed og eksplosionsevne | Pyridin er en meget brandfarlig væske (NFPA-klassificering=3), og dens dampe kan rejse en betydelig afstand og "glimme tilbage". Pyridindamp danner eksplosive blandinger med luft i koncentrationer på 1,8 til 12,4 % (efter volumen). Kuldioxid eller tørre kemiske ildslukkere bør anvendes til pyridinbrande. |
| Industrielle anvendelser | Pyridin er et godt opløsningsmiddel for en lang række forbindelser, både organiske og uorganiske (Windholz et al 1983). Omkring 50 % af pyridin, der bruges i USA, er til produktion af landbrugskemikalier, såsom herbiciderne paraquat, diquat og triclopyr og insekticidet chlorpyrifos. Andre anvendelser er i produktionen af piperidin; fremstilling af lægemidler, såsom steroider, vitaminer og antihistaminer; og som opløsningsmiddel. Anvendelse af opløsningsmidler findes i både den farmaceutiske og polycarbonatharpiksindustrien. Det er særligt anvendeligt som opløsningsmiddel i processer, hvor HC1 udvikles (Santodonato et al. 1985). Mindre anvendelser af pyridin er til denaturering af alkohol- og frostvæskeblandinger, som farvningsassistent i tekstiler og som smagsstof (Jori et al 1983; Furia 1968; HSDB 1988). |
| Kontaktallergener | Pyridin (usubstitueret pyridin) og dets derivat (substituerede pyridiner) er meget udbredt i kemi. Pyridin er et opløsningsmiddel, der bruges til mange organiske forbindelser og vandfri metalliske saltkemikalier. Indeholdt i Karl Fischer-reagens inducerede det kontakteksem hos en laboratorietekniker. Der observeres ingen krydsfølsomhed mellem disse forskellige stoffer. |
| Sikkerhedsprofil | Gift ad intraperitoneal vej. Moderat giftig ved indtagelse, hudkontakt, intravenøs og subkutan vej. Mildt giftig ved indånding. Et hud- og stærkt øjenirriterende middel. Mutationsdata rapporteret. Kan forårsage depression af centralnervesystemet, mave-tarmbesvær og lever- og nyreskader. En brandfarlig væske og farlig brandfare, når den udsættes for varme, ild eller oxidationsmidler. Alvorlig eksplosionsfare i form af damp, når den udsættes for ild eller gnister. Reagerer voldsomt med chlorsulfonsyre, chromtrioxid, dinitrogentetraoxid, HNO3, oleum, perchromater, ppropiolacton, AgClO4, H2SO4. Glødende reaktion med fluor. Reagerer for at danne pyrofore eller eksplosive produkter med bromtrifluorid, trifluormethylhypofluorit. Blandinger med formamid + jod + svovltrioxid er opbevaringsfarer og frigiver kuldioxid og svovlsyre. Uforeneligt med oxiderende materialer. Reagerer med maleinsyreanhydrid (over 150 grader) og udvikler kuldioxid. Brug alkoholskum til at bekæmpe brand. Når den opvarmes til nedbrydning, udsender den meget giftige dampe af NOx. |
| Potentiel eksponering | Pyridin anvendes som opløsningsmiddel i den kemiske industri og som denatureringsmiddel for ethylalkohol; som mellemprodukt i produktionen af pesticider; inden for lægemidler; ved fremstilling af maling, sprængstoffer, farvestoffer, gummi, vitaminer, sulfa-lægemidler; og desinfektionsmidler. |
| Kræftfremkaldende egenskaber | Pyridin var ikke kræftfremkaldende i flere kroniske subkutane undersøgelser. F344-rotter fik pyridin oralt i drikkevand i doser på 0, 7, 14 eller 33 mg/kg i 2 år. Den højeste dosis gav et fald i kropsvægt og vandforbrug. Øget renal tubulær adenom eller karcinom og tubulær hyperplasi blev observeret hos mænd ved 33 mg/kg. Øget mononukleær celleleukæmi blev observeret hos hunner ved 14 og 33 mg/kg, hvilket blev anset for tvetydigt med hensyn til forholdet til pyridineksponering, da dette er et almindeligt fund hos denne rottestamme. Koncentrationsrelateret ikke-neoplastisk ændring i leveren blev set ved 33 mg/kg. Wistar-hanrotter blev på lignende måde behandlet med doser på 0, 8, 17 eller 36 mg/kg i 2 år. Nedsat overlevelse og kropsvægt blev set ved 17 og 36 mg/kg. Forøgede testikelcelleadenomer blev set ved 36 mg/kg. Der blev ikke rapporteret ændringer i overlevelse eller neoplasma i andre væv, inklusive nyrerne, selvom øget nefropati og hepatisk centrilobulær degeneration/nekrose blev observeret hos nogle pyridinbehandlede rotter. |
| Kilde | Pyridin forekommer naturligt i kartofler, anabasis, henbaneblade, pebermynte (0 til 1 ppb), teblade og tobaksblade (Duke, 1992). Identificeret som en af 140 flygtige bestanddele i brugte sojabønneolier indsamlet fra et forarbejdningsanlæg, der stegte forskellige okse-, kylling- og kalvekødsprodukter (Takeoka et al., 1996). |
| Miljøskæbne | Biologisk.Heukelekian og Rand (1955) rapporterede en 5-d BOD-værdi på 1,31 g/g, hvilket er 58,7 % af ThOD-værdien på 2,23 g/g. En Nocardia sp. isoleret fra jord var i stand til at transformere pyridin i nærvær af semicarbazid til et mellemprodukt identificeret som ravsyresemialdehyd (Shukla og Kaul, 1986). 1,4-Dihydropyridin, glutarsyredialdehyd, glutarsyresemialdehyd og glutarsyre blev identificeret som mellemprodukter, når pyridin blev nedbrudt af Nocardia-stamme Z1 (Watson og Cain, 1975). Fotolytisk.Bestråling af en vandig opløsning ved 50 grader i 24 timer resulterede i et 23,06% udbytte af kuldioxid (Knoevenagel og Himmelreich, 1976). Kemisk/fysisk.Gasfasereaktionen af ozon med pyridin i syntetisk luft ved 23 grader gav et nitreret salt med formlen: [C6H5NH]+NO3 - (Atkinson et al., 1987). Ozonering af pyridin i vandige opløsninger ved 25 grader blev undersøgt med og uden tilsætning af tert-butylalkohol (20 mM) som radikalfjerner. Med tert-butylalkohol gav ozonering af pyridin hovedsageligt pyridin-N-oxid (80 % udbytte), som var meget stabilt over for ozon. Uden tert-butylalkohol spaltes den heterocykliske ring hurtigt under dannelse af ammoniak, nitrat og amidforbindelsen N-formyloxamsyre (Andreozzi et al., 1991). |
| Metabolisme | Pyridin absorberes gennem mave-tarmkanalen, huden og lungerne og elimineres via urinen, fæces, hud og lunger, både som metabolitter og som moderforbindelse (Jori et al 1983). Optagelse i væv øges med dosis, og eliminationen er bifasisk (Zharikov og Titov 1982; HSDB 1988). Eliminationen er hurtig, og der ser ikke ud til at være nogen vævsophobning (Jori et al. 1983). Observationen af His (1887) af urinudskillelsen af Af-methylpyridin fra pyridindoserede dyr var det første eksempel på Af-methylering. Kendte urinmetabolitter af pyridin hos pattedyr inkluderer nu pyridin-N-oxid, N-methylpyridin, 4-pyridon, 2-pyridon og 3-hydroxypyridin. Nogle metabolitter mangler stadig at blive identificeret (Damani et al. 1982). De relative mængder af metabolitterne er meget afhængige af arten og dosis (Gorrod og Damani 1980). For eksempel har rotten vist sig at udskille 70 % af en dosis på 1 mg/kg i urinen i de første 24 timer efter dosering, men det tal falder til kun 5,8 % for en dosis på 500 mg/kg (D'Souza et al. al 1980). Selvom urinudskillelse af pyridin og dets metabolitter ser ud til at være en væsentlig eliminationsvej, er ikke-urinudskillelse ikke blevet grundigt undersøgt (Santodonato et al. 1985). Hos kaniner har pyridin-N-methyltransferaseaktiviteten vist sig at være højest i lungecytosol, og det har vist sig at anvende 5-adenosylmethionin som methyldonor (Damani et al. 1986). Denne vej er mættelig i både rotter og marsvin (D'Souza et al. 1980). Produktet af denne reaktion, N-methylpyridin, er mindre kronisk giftigt, men mere akut giftigt end pyridin (Williams 1959). Pyridin-N-oxid produceres af cytochrom P-450-systemet, og aktiviteten induceres af phenobarbital- eller pyridinforbehandling, men ikke af 3-methylcholanthren (Gorrod og Damani 1979; Kaul og Novak 1987). Hos kaninen er den alkohol-inducerbare (og pyridin-inducerbare) P-450 LM3Aser ud til at være den lave Kmisozym, som katalyserer pyridin Af-oxidproduktion (Kim og Novak 1989). N-oxidationen af pyridin kan repræsentere en vej til bioaktivering (Santodonato et al. 1985), og denne vej bliver vigtigere, efterhånden som pyridindosis øges (Damani et al. 1982). |
| opbevaring | Pyridin bør kun anvendes i områder fri for antændelseskilder, og mængder større end 1 liter bør opbevares i tæt lukkede metalbeholdere i områder adskilt fra oxidationsmidler. |
| Forsendelse | UN1992 Brandfarlige væsker, giftige, nej, Fareklasse: 3; Etiketter: 3-Brændbar væske, 6.1-Giftige materialer, teknisk navn påkrævet. |
| Oprensningsmetoder | Sandsynlige urenheder er H2O og aminer såsom picolinerne og lutidinerne. Pyridin er hygroskopisk og er blandbart med H2O og organiske opløsningsmidler. Det kan tørres med fast KOH, NaOH, CaO, BaO eller natrium, efterfulgt af fraktioneret destillation. Andre metoder til tørring omfatter henstand med Linde type 4A molekylsigter, CaH2 eller LiAlH4, azeotropisk destillation af H2O med toluen eller *benzen, eller behandlet med phenylmagnesiumbromid i ether, efterfulgt af afdampning af etheren og destillation af pyridinen. En anbefalet [Lindauer Mukherjee Pure Appl Chem 27 267 1971]-metode tørrer pyridin over fast KOH (20g/Kg) i 2 uger og fraktioneret destillerer supernatanten over Linde type 5A molekylsigter og fast KOH. Produktet opbevares under CO2-frit nitrogen. Pyridin kan opbevares i kontakt med BaO, CaH2 eller molekylsigter. Ikke-basiske materialer kan fjernes ved at dampdestillere en opløsning indeholdende 1,2 ækvivalenter 20% H2SO4 eller 17% HCl, indtil ca. 10% af basen er blevet overført sammen med de ikke-basiske urenheder. Remanensen gøres derefter alkalisk, og basen fraskilles, tørres med NaOH og fraktionsdestilleres. Alternativt kan pyridin behandles med oxidationsmidler. Således er pyridin (800 ml) blevet omrørt i 24 timer med en blanding af ceriumsulfat (20 g) og vandfri K2CO3 (15 g), derefter filtreret og fraktioneret destilleret. Hurd og Simon [J Am Chem Soc 84 4519 1962] omrørte pyridin (135mL), vand (2,5L) og KMnO4 (90g) i 2 timer ved 100o og henstod derefter i 15 timer før de filtrerede de udfældede manganoxider fra. Tilsætning af fast KOH (ca. 500 g) fik pyridin til at separere. Det blev dekanteret, tilbagesvalet med CaO i 3 timer og destilleret. Adskillelse af pyridin fra nogle af dets homologer kan opnås ved krystallisation af oxalater. Pyridin udfældes som dets oxalat ved at tilsætte det til den omrørte opløsning af oxalsyre i acetone. Bundfaldet filtreres, vaskes med kold acetone, og pyridin regenereres og isoleres. Andre metoder er baseret på kompleksdannelse med ZnCl2 eller HgCl2. |
| Uforeneligheder | Voldsom reaktion med stærke oxidationsmidler; stærke syrer; chlorsulfonsyre; maleinsyreanhydrid; oleum jod. |
| Bortskaffelse af affald | Kontrolleret forbrænding, hvorved nitrogenoxider fjernes fra udløbsgassen ved hjælp af skrubber, katalytiske eller termiske anordninger. |
| Pyridinpræparationsprodukter og råmaterialer |
| Råmateriale | Sulfuric acid-->Ammonia-->Benzene-->COAL TAR-->3-Picoline-->COKEOVENGAS-->1,5-DIAMINOPENTAN DIHYDROCHLORID |
| Forberedelsesprodukter | Methyl 2-Fluoroisonicotinate-->2-ACETYL-5-CYANOTHIOPHENE-->5-BROMO-2-FLUOROCINNAMIC ACID-->4-NITROISOPHTHALIC ACID-->3,5-DIMETHOXYCINNAMIC ACID-->2-(2-Butoxyethoxy)ethyl acetate-->2,4-MESITYLENEDISULFONYL DICHLORIDE-->(4-FLUORO-BENZYL)-METHYL-AMINE-->1-Phenacylpyridinium bromide-->3-(TRIFLUOROMETHOXY)CINNAMIC ACID-->trans-Ferulic acid-->3-(Trifluoromethyl)pyrazole-->4-Fluorocinnamic acid-->Indigosol Green Blue IBC-->2-Amino-4-methyl-5-acetylthiazole-->Benzyl 2-chloroacetate-->5-ACETAMIDONICOTINIC ACID-->7-ACETOXYCOUMARIN-->2-AMINO-4-METHYL-QUINOLINE-3-CARBONITRILE-->N-PHENYLISONICOTINAMIDE-->Allyl methyl carbonate-->Pyridine-3-sulfonyl chloride hydrochloride-->Syringaldehyde-->2,4,5,6-TETRAMETHYLBENZENEDISULFONYL DICHLORIDE-->3-(3-METHYL-2-THIENYL)ACRYLIC ACID-->Vat Grey M-->17beta-Hydroxy-17-methylandrosta-4,9(11)-dien-3-one-->butyl N-phenylcarbamate-->3-Methoxycinnamic acid-->1-CHLORO-2-METHYLPROPYL CHLOROFORMATE-->Pyrazinecarbonitrile-->2-AMINO-6-CHLORO-3,5-DICYANOPYRIDINE-->4-BROMO-TETRAHYDROPYRAN-->Phenylcarbamic acid propyl ester-->Hydrocortisone acetate-->5-METHYLPICOLINIC ACID-->4-Acetamido-2-chloropyridine-->Pyridinium p-Toluenesulfonate-->1,2,4-Triazolo[4,3-a]pyridin-3(2H)-one-->Paraquat dichlorid |
Populære tags: pyridin, Kina pyridin producenter, leverandører, fabrik
Du kan også lide
Send forespørgsel







